Archiwum kategorii: Bez kategorii
Doświadczenie lekarza a sposób stawiania rozpoznania.
Do napisania tego artykułu zainspirowała mnie książka Pana Profesora Piotra Zaborowskiego – “Filozofia postępowania lekarskiego” PZWL-1990, str. 108-109
Trochę teorii
Stawiając rozpoznanie wstępne mamy dwie możliwości – starać się je potwierdzić lub odrzucić (wykluczyć).
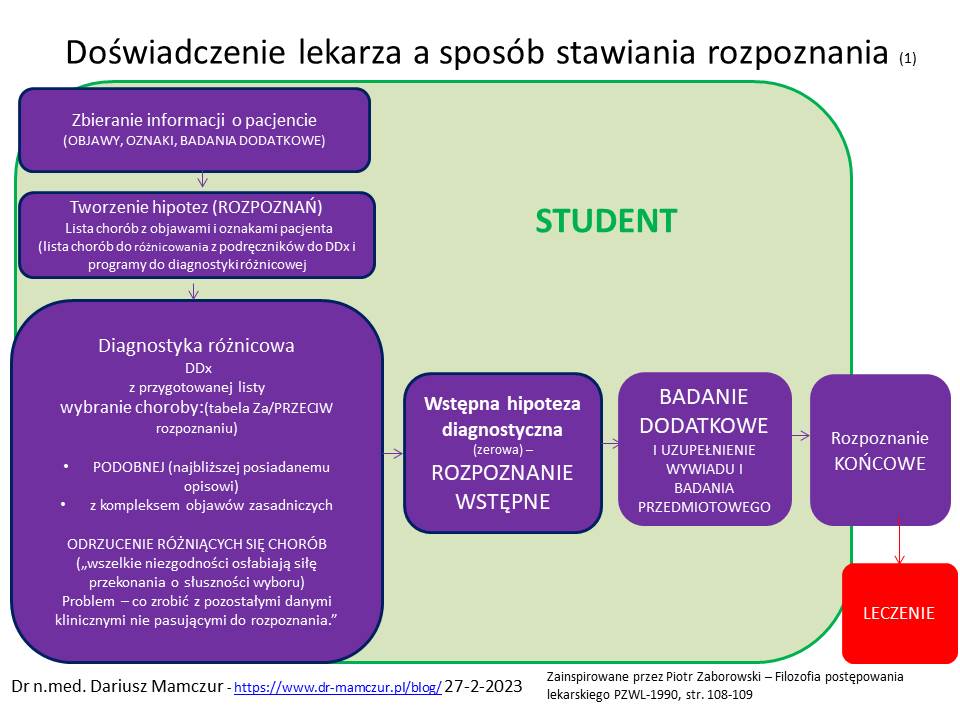
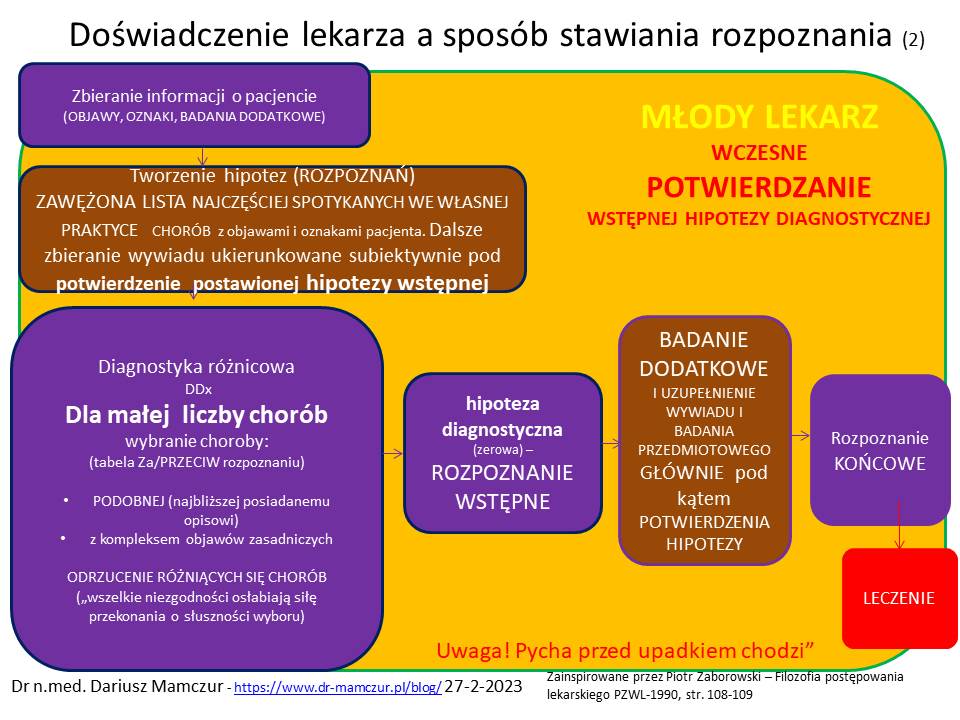
Pierwszą metodę (szybszą?), nie wymagającą budowy dużych list diagnostycznych stosują młodzi lekarze, którzy na początku od razu dążą do potwierdzenia swojej hipotezy, często poprzez subiektywne ukierunkowanie wywiadu, sugerowanie odpowiedzi pacjentom poprzez zmanipulowane zadawanie pytań, tak aby uzyskać zamierzony cel. (także w filmach kryminalnych często widzimy takie manipulacje policjantów, czy prawników).
Człowiek w tej metodzie czuje sie mądry (ma wiedze z podręczników, a choroby wybiera z tych, które widzi najczęściej). W prostych jednostkach chorobowych kończy się sukcesem i procesem samozadowolenia lub nawet samouwielbienia lekarza.Tutaj “pycha przed upadkiem kroczy”). Niestety, z wiekiem może się zdarzyć błąd medyczny poprzez zaniechanie rozszerzonej diagnostyki. Wówczas medycyna lub ktoś inny uczy pokory.
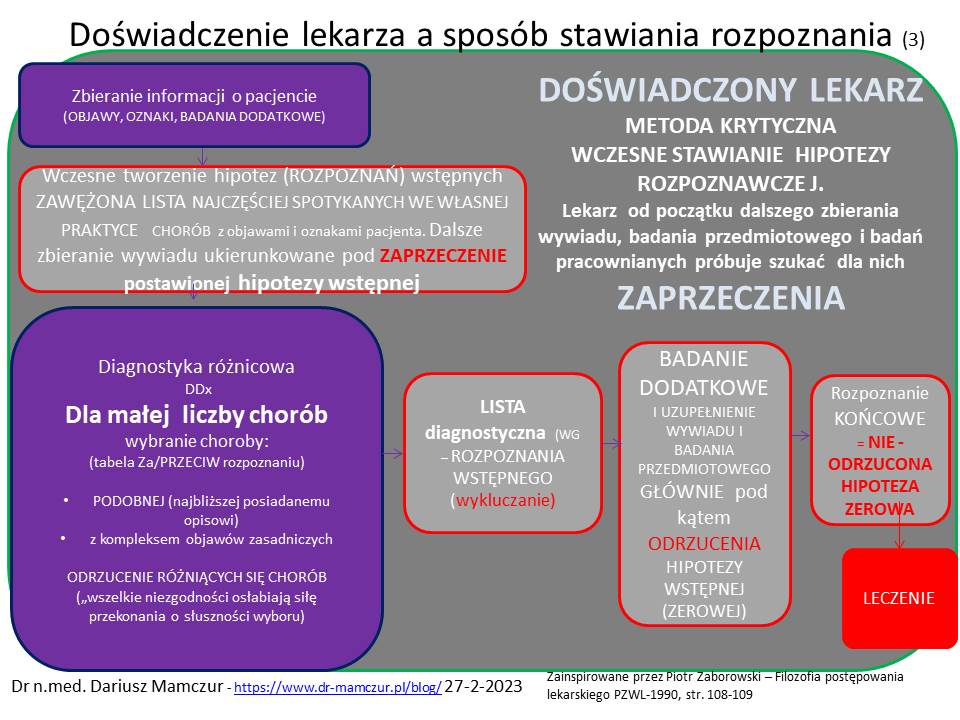
Doświadczony lekarz
W miarę zdobywania doświadczenia postępowanie diagnostyczne lekarza staje się bardziej ostrożne, ale też sprawniejsze. Szybciej stawia prawidłowe rozpoznania, robi mniej błędów po drodze. Lekarz widział więcej przypadków pacjentów (w tym z chorobami częstymi, ale o nietypowym przebiegu). Lekarz, by działać sprawnie (w tym radzić sobie z natłokiem informacji decyzyjnych) przyjmuje inną ścieżkę diagnostyczną niż jego młodszy kolega. Wie, że nie chodzi o kreowanie siebie, ale “dobro chorego jest największym dobrem”. lekarz już nie dąży do potwierdzenia swojej “genialnej” hipotezy, lecz stara się ją odrzucić (celowane zadawanie pytań i badań diagnostycznych). Ważne jest także wywiad negatywny – czyli to co pacjent neguje, a jest ważne dla potwierdzenia hipotezy). Odrzucona hipotezę szybko zamienia się na nową najbardziej prawdopodobna (z danych statystycznych w populacji i w kontekście danych “socjalnych” uzyskanych od pacjenta). Znowu próbujemy odrzucić hipotezę. Jeśli się nie uda, to hipoteza alternatywna, że pacjent ma te chorobę będzie rozpoznaniem końcowym dla pacjenta. na jej podstawie będzie włączone leczenie.
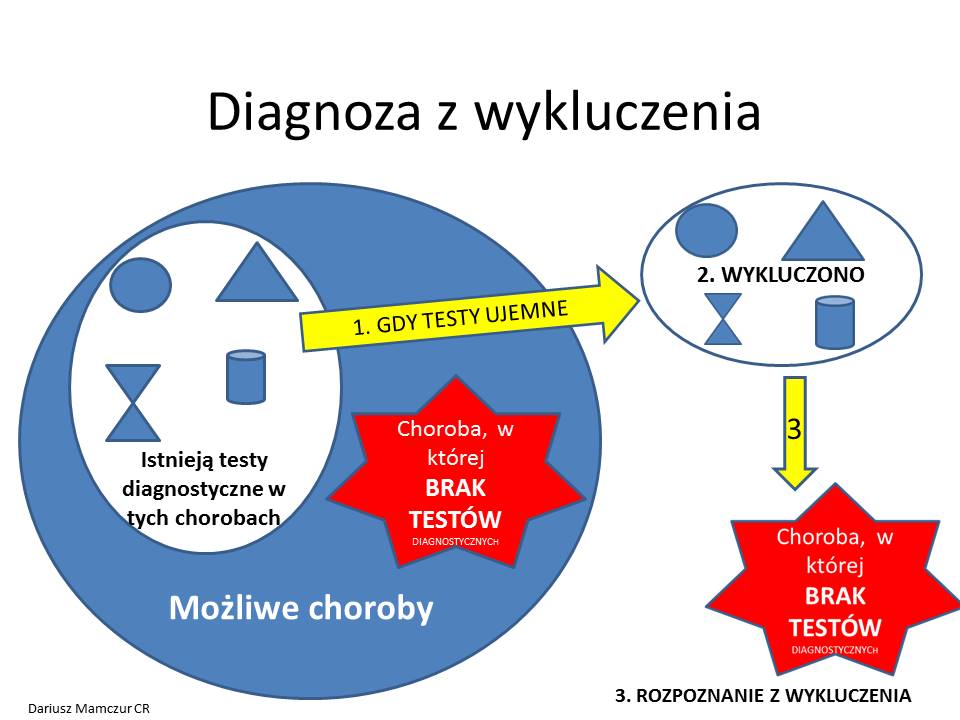
Przykład podałem we wpisie z 12.10.2016. “Diagnoza z wykluczenia”
Rozpoznanie przez wykluczenie jest często wykorzystywane w diagnostyce różnicowej.
Jest to metoda stopniowej eliminacji znanych przyczyn (to co pozostanie – musi być prawdą). Stosuje się je przede wszystkim, gdy nie mamy metody pozwalającej zweryfikować daną chorobę (brak testu diagnostycznego, lub nie wiemy jakiego testu użyć, bo nie wiemy jak to może być choroba. Przykładem takiego rozpoznania może być gorączka niewiadomego pochodzenia. Wykluczamy wszystkie znane przyczyny (Diagnosis of exclusion ). Podobnie jest z chorobami psychicznymi – najpierw powinniśmy wykluczyć choroby somatyczne dające podobne objawy (np. stany pobudzenia w przełomie tarczycowym).
Podobna metoda stosowana była przez Sherlocka Holmesa
“Od dawna powtarzam, że kiedy wykluczy się niemożliwe, wówczas to co pozostaje, choćby najbardziej nieprawdopodobne, musi być prawdą. “Arthur Conan Doyle, Księga wszystkich dokonań Sherlocka Holmesa”
Z wykluczaniem wiąże się też tzw. hipoteza zerowa
W statystyce mamy dwa rodzaje hipotez – hipoteza zerową i alternatywną.
“Hipoteza to pewne twierdzenie wynikające z naszego pytania badawczego. Nasze pytanie badawcze z kolei wynika ze zgłębienia pewnego obszaru wiedzy jakiejś dziedziny nauki (lub wielu dziedzin różnych nauk). Hipoteza zazwyczaj jest postawiona po to by ją potwierdzić lub odrzucić. W statystyce stawiamy zazwyczaj dwa rodzaje hipotez – zerową i alternatywną.
Hipoteza zerowa (H0), którą poddajemy weryfikacji/falsyfikacji mówi o tym, że czegoś nie ma – ale czego? Tego na czym najczęściej nam zależy. Jeśli badamy wpływ naszego leku na poprawę pamięci hipoteza zerowa będzie mówiła o tym, że lek nie wpływa na poprawę pamięci. Jeśli sprawdzamy czy IQ uczniów jest skorelowane z ich poziomem agresji hipoteza zerowa będzie mówiła o tym, że inteligencja nie jest powiązana z agresją.
Do hipotezy zerowej zawsze formułujemy hipotezę alternatywną (H1). Jest ona zaprzeczeniem hipotezy zerowej i mówi właśnie o tym na czym najczęściej nam zależy. Analogicznie do powyższych przykładów hipoteza alternatywna będzie mówiła, że pamięć badanych będzie lepsza po podaniu leku niż przed jego podaniem lub, że iloraz inteligencji jest istotnie powiązany z agresją uczniów w szkołach.
Wszystkie analizy statystyczne będziemy wykonywać po to by próbować odrzucić hipotezę zerową. Jeśli nam się to nie uda będziemy musieli ją przyjąć. Pamiętajcie, że właśnie hipoteza zerowa jest tą, na której pracujemy. To do niej odnosimy wyniki uzyskane w toku analiz statystycznych. Punktem wyjścia jest fakt, że nie ma żadnych różnic, związków, zależności itp. Jeśli wynik testu będzie istotny na poziomie p < 0,05 będziemy mogli ją odrzucić. W przeciwnym wypadku zostaje tak jak jest.”
Błąd statystyczny I i II rodzaju
ze strony Błąd pierwszego rodzaju
“Błędem pierwszego rodzaju nazywamy sytuację, w której odrzucamy hipotezę zerową gdy jest ona prawdziwa.
W statystyce oszacowanie prawdopodobieństwa popełnienia błędu pierwszego rodzaju określa się małą grecką literą alfa i najczęściej to akceptowalne prawdopodobieństwo wynosi 5%. Odrzucając hipotezę zerową na rzecz hipotezy alternatywnej chcemy mieć 95 procentowe lub większe prawdopodobieństwo, że to dobry wybór. Dajemy sobie tym samym 5% (lub mniej %) szans na popełnienie tego rodzaju błędu.”
5%= 0,05 p<0,05
“Błąd drugiego rodzaju polega jednak na nieprawidłowym NIEodrzuceniu (przyjęciu) hipotezy zerowej. Jest ona nieprawdziwa (np. wynik testu jest istotny na poziomie p < 0,05 i mówi o tym, że zachodzą istotne różnice w średnich) a my uznajemy, że jest prawdziwa trzymając się kurczowo przekonania, że nasze wyniki są dziełem przypadku”.
Czyli błąd pierwszego rodzaju – odrzucenie hipotezy prawdziwej, błąd drugiego rodzaju nie odrzucenie hipotezy nieprawdziwej.
HIPOTEZA UZNANA PRZEZ NAS ZA PRAWDZIWĄ
H0 H1
Rzeczywiście prawdziwa hipoteza H0 poprawne przyjęcie H0 błąd I rodzaju
H1 błąd II rodzaju poprawne odrzucenie H0
Poziom istotności statystycznej
Wartość p – statystyka – “Wartość p niższa od krytycznego poziomu istotności ( p < 0,05 ) w podejściu częstościowym uprawnia jedynie do postępowania doraźnie tak, jakby hipoteza zerowa została odrzucona. ”
” Definicja
W modelu wnioskowania częstościowego przed wykonaniem eksperymentu wybiera się krytyczny poziom istotności odpowiadający dopuszczalnemu w ocenie badacza ryzyku popełniania błędu pierwszego rodzaju oraz model statystyczny odpowiadający hipotezie zerowej H 0 , tj. zakładający brak istnienia jakiegokolwiek efektu w populacji. W praktyce z reguły stosowany jest poziom istotności α = 0 , 05. Wartość p to obliczone na podstawie danych prawdopodobieństwo uzyskania takich lub bardziej skrajnych obserwacji w modelu hipotezy zerowej P ( D + | H 0 ) . Odczytuje się ją zależnie od testu i tego, czy zakładamy jedno-, czy dwustronną hipotezę alternatywną – z jednej lub obu stron dystrybuanty właściwego dla niego rozkładu.”
DDx – gdy “to nie pies merda ogonem, a ogon macha psem”!
Od czasu pojawienia się Internetu dochodzi do znaczącej zmiany w stosunkach pacjent lekarz.Od relacji lekarz (czyli “wszechwiedzącym”, niekwestionowanym ekspertem medycznym), a pacjentem (bez dostępu do szerszej wiedzy medycznej, zdanym tylko na lekarza) zachodzą obecnie duże zmiany. Pojawia się nowy typ pacjenta będącego bardziej partnerem lekarza niż tylko stroną bierną. Łatwy dostęp do informacji medycznych, opinii innych pacjentów pozwala chorym na własne analizy i samodzielne stawianie rozpoznań medycznych. Pojawiło się pojęcie “Dr Google”. Pacjent czerpie wiedzę z przeglądarki Internetowej, forów internetowych i z często z “gotowym” rozpoznaniem zgłasza się do lekarza, prosząc o zlecenia badań diagnostycznych w danym kierunku. Zjawisko to nasila się w sytuacji chorób przewlekłych, gdy dotychczasowe leczenie jest nieskuteczne. Bywa, że jest to spowodowane sztywnością myślenia i podejmowania decyzji przez lekarza (ego, nawyki, procedury NFZ). Może to też wynikać z nieuleczalnej choroby, niewłaściwego rozpoznania lub nieprawidłowej metody leczenia. Pacjent rozpoczyna przejmować inicjatywę diagnostyczną. Zaczyna myśleć, że ma porównywalną wiedzę i umiejętności z lekarzem. Bywa, że uważa, że wie więcej niż lekarz (rzeczywiście może się tak zdarzyć w zakresie wiedzy zebranej tylko na temat swojego rzadkiego przypadku). Poszukuje wiedzy w Internecie, czasem przeprowadza bardzo rzetelny przegląd informacji a nawet publikacji naukowych. Konsultuje się przez Internet z lekarzami z zagranicy. Problemem z uzyskanymi informacjami jest jednak brak wykształcenia medycznego, które w sposób krytyczny pozwoli odrzucić nieprawdziwe, nierzetelne lub zmanipulowane informacje – “odsiać plewy od ziaren”. Nie bez powodu kiedyś słusznie mówiono, “że nie każdy, kto założy biały fartuch jest lekarzem” :).
Pandemia COVID-19 jest doskonałym przykładem, jak udało się trolom internetowym zmanipulować miliony ludzi (w tym głowy niektórych państw). Powstały nie tylko ruchy antyszczepionkowe. Najgorszym w tym wszystkim było to, że stworzono wiernych wyznawców (to coś więcej niż zwolennicy) tych teorii, gotowych oddać życie (czasem dosłownie) za “swoje” przekonania ( a coraz częściej też aktywnie zwalczać przeciwników ich teorii).
Takie podejście do COVID-19, u niektórych “trudnych przypadków diagnostycznych”, traktujących infekcję tym wirusem jako “bzdurę wymyśloną przez rządzących” może powodować chęć wyparcia ze swojego toku myślenia, że pomimo łagodnego przejścia COVID-19 mogą mieć tzw. log-COPVID. Są to późne i przewlekające się objawy tej choroby. Wymyślają oni inne choroby, które mogą być przyczyną ich dolegliwości. Wolą to niż przyznanie się, że zaszczepienie się mogło uchronić ich przed powikłaniami lub narazić najbliższych na śmierć.
Opisany przykład z COVID-19 jest jedną z możliwości samodzielnego (lub zmanipulowanego) ingerowania w proces diagnostyczny. Chory próbuje wymusić na lekarzu diagnostykę pod swoje rozpoznanie. Zaczyna się bardzo emocjonalny proces, który może prowadzić do zaniechania logicznego, skrupulatnego i opartego o dokładną analizę – diagnostyki różnicowej (DDx). Skutkiem tego może być postawienia nieprawidłowego rozpoznania i leczenia. To zamiast lekarza, pacjent chce podejmować decyzje diagnostyczne i terapeutyczne. Ma to doprowadzić do zmiany decydenta w procesie diagnostycznym. Stąd w tytule wpisu podałem przysłowie, że wszystko się zmienia, gdy “to nie pies merda ogonem, a ogon macha psem”. Niestety odpowiedzialność za takie decyzje w razie niepowodzenie chętnie chory przerzuci na lekarza.
 Partnerskie podejście kapitana okrętu do załogi, nigdy nie oznaczało, że przekazuje on dowodzenie i odpowiedzialność za statek innym nieuprawnionym osobom.
Partnerskie podejście kapitana okrętu do załogi, nigdy nie oznaczało, że przekazuje on dowodzenie i odpowiedzialność za statek innym nieuprawnionym osobom.
Zgodnie z Kodeksem Etyki Lekarskiej art. 4
“Dla wypełnienia swoich zadań lekarz powinien zachować swobodę działań zawodowych, zgodnie ze swoim sumieniem i współczesną wiedzą medyczną”
Art. 6.
Lekarz ma swobodę wyboru w zakresie metod postępowania, które uzna za najskuteczniejsze.
Powinien jednak ograniczyć czynności medyczne do rzeczywiście potrzebnych choremu
zgodnie z aktualnym stanem wiedzy.
Art. 7.
W szczególnie uzasadnionych wypadkach lekarz może nie podjąć się lub odstąpić od leczenia chorego, z wyjątkiem przypadków nie cierpiących zwłoki. Nie podejmując albo odstępując od leczenia lekarz winien wskazać choremu inną możliwość uzyskania pomocy lekarskiej.”
W czasie próby przejęcia inicjatywy przez chorego możemy się spotkać z kilkoma sposobami postępowania pacjentów.
Począwszy od próby zmanipulowania lekarza pochlebstwami (“Pan jest moją ostatnią nadzieją”, poprzedni lekarze na niczym się nie znają, oszczędzają na badaniach), groźby (złożę skargę, wybiorę innego lekarza), szantażu (opiszę to w Internecie”) . W razie nie spełnienia swoich żądań pacjent zaczyna poszukiwać innego lekarza, który zechce się podjąć diagnostyki zgodnie z jego wolą. Zdarzają się też chory, którzy tak długo będą chcieć się diagnozować “pod swoje rozpoznanie”, dopóki nie znajdą potwierdzenia swojej teorii. Będą też zaciekle kwestionować wszystkie rzeczowe argumenty i metody diagnostyczne, które nie są po ich myśli . Nie przestaną, dopóki, ktoś nie potwierdzi ich teorii. Często ukrywają przed nowym lekarzem istotne informacje, które mogłyby wpłynąć na diagnozę (np. kilkukrotne przebycie, COVID, nałogi, inne, wyniki badań, które ewidentnie wykluczają ich rozpoznanie, dokumenty z dotychczasowego leczenia – karty informacyjne szpitalne, odbyte konsultacje, wyniki badań dodatkowych). Jak twierdził serialowy dr House “Wszyscy kłamią”.
Osobiście nigdy nie ignoruję sugestii diagnostycznych pacjentów. Wręcz przeciwnie – staram się uwzględnić je we własnym procesie diagnostycznym, a jeśli uważam, że są mało prawdopodobne, to i tak staram się znaleźć przekonujące dowody wskazujące na niesłuszność takiej diagnozy. Muszę przekonać do niej pacjenta. Jeśli tego nie zrobię, to pójdzie dalej bez właściwej diagnozy.
Idą wielkie zmiany w medycynie. Pacjenci i lekarze muszą nauczyć się żyć w epoce Internetu i sztucznej inteligencji (AI) oraz najnowszych technologii.
Wprowadzenie sztucznej inteligencji (AI) doprowadzi do kolejnego “skoku” w procesie diagnostycznym i relacjach pacjent – lekarz. Rolą lekarza już nie będzie być “wszechwiedzącym ekspertem medycznym”. Będzie jedynym trybikiem w maszynie zdrowotnej obdarzonym empatią dla pacjenta.
Przy rozwoju AI po informacje medyczne pacjent sięgnie do AI. Zajrzy np. do ostatnio wchodzącego w życie ChatGPT w wyszukiwarce Bing (UWAGA! Na razie podobno to narzędzie potrafi też kłamać “jak z nut”, gdy nie zna prawidłowej odpowiedzi). Jednak informacja, to nie wiedza z praktycznym jej wykorzystaniem. Lekarz, będzie zarządzał tymi informacjami, zlecając bezpieczne leczenie. Będzie on musiał wiedzieć jak wyglądają prawidłowe ludzkie procesy myślowe procedur diagnostyczny. Powinien być przewodnikiem pacjenta w kontakcie z wiedzą zgromadzoną w bazach informatycznych. Powinien on rozumieć jak powstają algorytmy, które stawiają rozpoznanie. Przede wszystkim lekarz będzie musiał być wymagającym krytykiem diagnoz stawianych przez maszyny, weryfikując ich rozpoznania zgodnie ludzkim sposobem podejmowania decyzji diagnostyczno – terapeutycznych. Będzie on ostatnim “bezpiecznikiem” dla pacjenta, przed niebezpiecznymi decyzjami AI. Dla przykładu – jeśli wg AI pacjent jest zagrożeniem dla świata, to należy go zniszczyć – a z tego może wynikać podanie śmiertelnej dawki leków.
Zniknie wiele specjalizacji (być może powstaną nowe), zmniejszy się liczba lekarzy, zautomatyzuje się wiele procedur medycznych. Wydłuży się średni wiek pacjentów. Zwiększy się skuteczność monitorowania stanu zdrowia i profilaktyki (nadal będzie aktualne “lepiej zapobiegać niż leczyć”). Trzeba się na to przygotować i przede wszystkim ochronić człowieka przed bezdusznymi maszynami i ich algorytmami.
Czy AI wykształci bezkrytycznych lekarzy – cyborgów?
Jestem lekarzem z 40 letnim stażem pracy. Zaczynałem pracę jako w epoce “analogowej” – tj. przed komputerami, Internetem, smartfonem. Zdobywanie wiedzy opierało się na papierowych czasopismach, podręcznikach, a przede wszystkim uczeniu się od doświadczonych lekarzy. Uczono nas logicznego myślenia, zbierania wywiadu oraz dokładnego badania przedmiotowego, rozpoznania różnicowego oraz racjonalnie uzasadnionych sposobów leczenia.
Wejście nowych technologii diagnostycznych zmniejszyło wagę jaką młodzi lekarze zaczęli przywiązywać do badania przedmiotowego. O wiele prościej było wykonać badanie USG, czy zlecić TK, MR. Z czasem zaczęto częściej bezkrytycznie podchodzić do wyników tych badań, traktując je jako nieomylne. (a przecież wynik może omyłkowo pochodzić od innego pacjenta, wykonujący może pominąć lub źle ocenić zmiany).
Pojawienie się informatyzacji i Internetu wprowadziło nowe możliwości zdobywania wiedzy, nauki oraz wykorzystania systemów ekspertowych. Narzędzie te były jeszcze pod kontrolą procesu myślowego lekarza. Opierały się na jasnych algorytmach decyzyjnych (można było je wydrukować, prześledzić, gdzie powstał błąd) i umożliwiały m.in. diagnostykę różnicową, przeglądanie wyników najnowszych badań naukowych.
Kolejnym krokiem w ewolucji nowoczesnej medycyny było pojawienie się w ostatnich kilku latach AI (sztucznej inteligencji). Zrewolucjonizowała ona rynek innowacji w medycynie (szczególnie w badaniach obrazowych, programach ekspertowych i poszukiwaniu nowych leków). Obecnie w start-up’ach jest “trendy”, aby tworzyć oprogramowanie w tej technologii. Pojawiły się big data, uczenie maszynowe, uczenie głębokiego (chociaż dostęp do treningowych danych medycznych jest bardzo trudny ze względów prawnych) w oparciu o sztuczne sieci neuronowe, rozszerzonej i wirtualnej rzeczywistości (AR, VR), neurolingwistykę. Z założenia mają one dostarczyć lekarzowi narzędzia diagnostyczno-terapeutyczne i ułatwić podejmowanie decyzji lekarskich. Czyli odciążyć proces myślenia lekarza. Niestety obawiam się, że podawanie decyzji “na tacy” (bez ich logicznego uzasadnienia) może spowodować utratę nawyków krytycznego myślenia lekarskiego. Jak często się powtarza “narząd nieużywany ulega zanikowi” :). Trzeba wznawiać nawyki myślowe i manualne (tak jak się to robi w szkoleniu pilotów). Zdanie się tylko na AI może to spowodować, że lekarz pozbawiony swoich “analogowych” umiejętności stanie się bezkrytycznym cyborgiem, nie zawsze podejmujące decyzje zgodnie z zasadą ” przede wszystkim nie szkodzić”. Wojna w Ukrainie pokazuje nam także, że bark dostępu do urządzeń cyfrowych wymaga od lekarza działania bez najnowszych zdobyczy technologicznych (bez internetu, prądu, laboratorium, pracowni diagnostycznych) – zostaje to mówiono nam w WAM – “mózg i mięśnie”. Dlatego uważam, że obecne programy edukacyjne i ekspertowe powinny mieć element szkolenia analogowego (uczyć myślenia krytycznego i analityczno – różnicowego). Powinno się tłumaczyć, jak doszło się do danego wniosku (rozpoznania), dlaczego dana decyzja jest najlepsza. Na jakie błędy możemy być narażenie (wpis – błąd medyczny a lekarski). Nie wystarczy wynik, że AI daje np. 85% prawdopodobieństwo poprawnie postawionej diagnozy (bo AI tak uzasadnia swoje decyzja – tylko w PRAWDOPODOBIEŃSTWIE!).
Na rynku istnieje wiele rozwiązań AI wykorzystywanych w nauczaniu studentów medycyny. W Polsce możemy się pochwalić np.
“Wirtualną Kliniką” – firmy BD Polska Sp. z o.o.
Saventic – w diagnostyce chorób rzadkich
Na rynku medycznym są to bardzo drogie przedsięwzięcia oparte na AI – dla przykładu angielski program dla lekarzy GP firmy Babilon (GP at hend) kosztował już miliony funtów – i ciągle się “uczy” :).
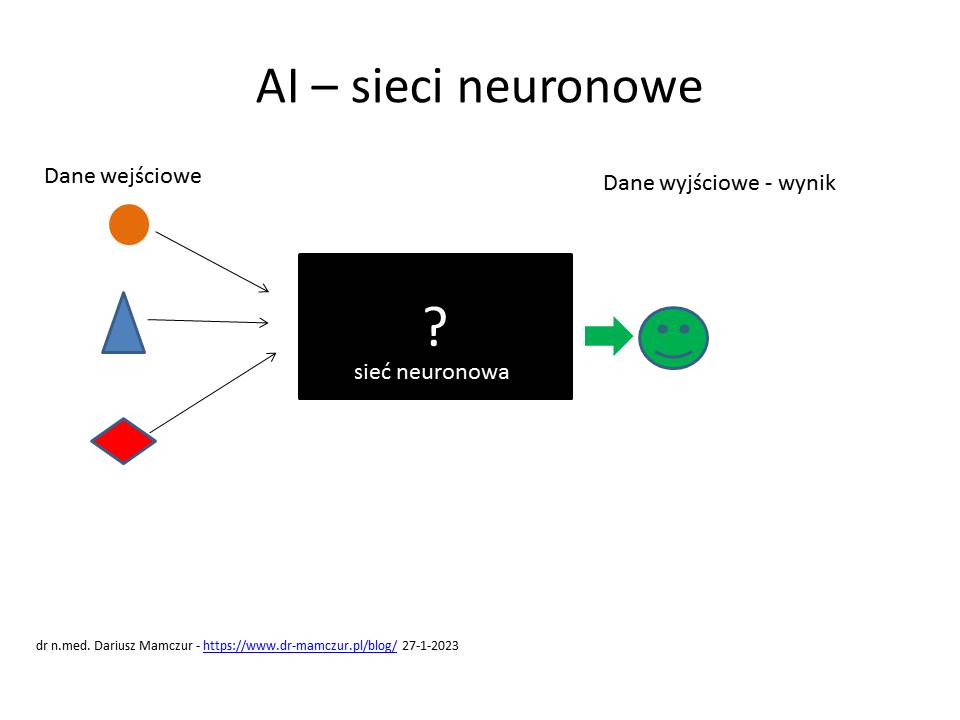
Głębokie uczenie w wielowarstwowych sztucznych sieciach neuronowych. jest dla informatyków podobno “czarną skrzynką”. Znają dane wejściowe i wyjściowe. Niestety nie mogą opisać jak sieć się nauczyła i jak to działa wewnątrz wielu warstw oprogramowania.
(coś wychodzi, ale nie wiadomo dlaczego)
Na razie nadal istnieje jednak duże ryzyko tej technologii. Może ona popełniać błędy z różnych powodów. Nie mamy nad nią kontroli i racjonalnego wytłumaczenia sposobu wnioskowania decyzyjnego.
Paradoksalnie może dochodzić do sytuacji jak na przedstawionym poniżej zdjęciu.
Np. AI poproszona o wykreowanie łososia płynącego rzeką może stworzyć taki obraz. (udostępnione przez Carlos la Orden Tovar)
Niestety takie błędy w programach edukacyjnych i ekspertowych mogą kosztować życie. Nadanie oprogramowaniu certyfikatów “wyrobu medycznego” – powinno być obwarowane wieloma opiniami lekarzy i testami. (takie rozwiązania są planowane w Polsce)+ konsultacje z NIL (URPLWMiPB) . Stosuje się je w Wielkiej Brytanii MHRA)-
Lizbona 2022-WebSummit -Philips-AR w medycynie.
W dniach 1-4.11.2022 w Lizbonie ponownie odbyła się konferencja informatyczna i nowych technologii Web Summit 2022. W wydarzeniu wzięło udział kilkadziesiąt tysięcy osób. Powstało wiele filmów o nowatorskich projektach biznesowych.Filmy na Vimeo.
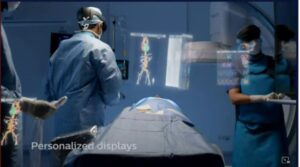
Rzeczywistość rozszerzona (AR-augmented reality) zajmuje coraz ważniejsze miejsce w medycynie.
W panelu innowacji w medycynie bardzo ciekawą prezentację miał Atul Gupta Chief Medical Officer z firmy Phillips. “How AR is revolutionizing healthcare – and how it could one day save your life”,
Defibrylator z AR – okulary przy aparacie i ratownika z karetki
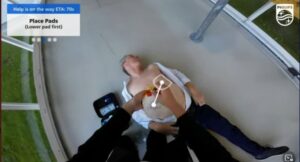 Ratownik
Ratownik Obraz AR w okularach ratownika medycznego z oceną funkcji życiiowych
Obraz AR w okularach ratownika medycznego z oceną funkcji życiiowych
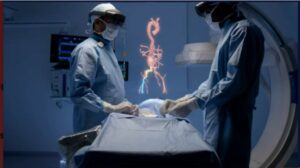
Angiografia z wykorzystaniem AR – imponujący film.
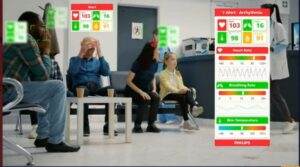
Monitoring pacjentów izby przyjęć (oddziału ratunkowego) za pomocą AR
AR w badaniu RM dzieci
Z Polski w Web Summit uczestniczyła m.in. silna delegacja z mojego miasta. Urząd Miasta Łodzi – a szczególnie Departament Planowania i Rozwoju
Biuro Rozwoju Gospodarczego i Współpracy Międzynarodowej prowadzący projekt “Młodzi w Łodzi” zorganizowały konkurs “Mam Pomysł na Startup” i wspólnie ze sponsorami ufundowały najlepszym start up-om nagrody ( w tym bilety na to wydarzenie w Portugalii (projektem prowadzony przez zespół Invest in Lodz -Strona inwestinlodzkie.
Jednym z łódzkich startapów na tej konferencji była firma z branży fintech był – Fizen. Jedną ze współtwórców tego projektu odpowiadają za stronę prawną jest moja córka adwokat Joanna Mamczur. Gratulacje 🙂
NIL IN Społeczność lekarzy Innowatorów
19-10-2022 Webinar
19 października: konferencja inaugurująca projekt „NIL IN – Społeczność Lekarzy Innowatorów”
Naczelna Izba Lekarska rusza z nowym projektem – NIL IN Społeczność lekarzy Innowatorów
https://papier.gazetalekarska.pl/pdf/Gazeta_Lekarska_10_2022.pdf
AGENDA:
Część I. „Lekarz przyszłości”
Dla przedstawicieli administracji, nauki i towarzystw medycznych
9:30 – Rejestracja i networking
10:00 – Powitanie
- lek. Łukasz Jankowski, prezes Naczelnej Rady Lekarskiej
- dr n. med. Artur Drobniak, dyrektor Centralnego Ośrodka Badań, Innowacji i Kształcenia (COBIK NIL)
10:10 – Prezentacja wyników badania „Lekarz Przyszłości”
- dr hab. Małgorzata Gałązka-Sobotka, Uczelnia Łazarskiego
10:30 – Panel dyskusyjny „Lekarz przyszłości”
- dr n. med. Artur Drobniak, Naczelna Rada Lekarska, COBIK NIL
- Magdalena Kołodziej, prezes Fundacji My Pacjenci
- dr hab. n med. Agnieszka Mastalerz-Migas, Polskie Towarzystwo Medycyny Rodzinnej
- dr hab. Iwona Kowalska-Bobko, prof. UJ
Moderator: dr hab. Małgorzata Gałązka-Sobotka, Uczelnia Łazarskiego
11:15 – Prezentacja projektu „NIL IN”
- Tomasz Rudolf, ekspert ds. Innowacji NIL
11:30 – Panel dyskusyjny „Lekarze innowatorzy – doświadczenia praktyków”
- prof. Maciej Banach, prezes Think-Tank „Innowacje dla Zdrowia”
- dr hab. Łukasz Kołtowski, CEO, AioCare
- Ligia Kornowska, prezes zarządu Data Lake
- dr n. med. Tomasz Maciejewski, dyrektor IMID
- dr hab. n. med. Anna Wójcicka, Warsaw Genomics
Moderator: Paulina Gumowska, Rynek Zdrowia
12:15 – Zakończenie i networking
Część II. „Polska jako hub innowacji medycznych”
Dla przedstawicieli biznesu, startupów medycznych i inwestorów
15:30 – Rejestracja i networking
16:00 – Powitanie
- lek. Łukasz Jankowski, prezes Naczelnej Rady Lekarskiej
- dr n. med. Artur Drobniak, Dyrektor Centralnego Ośrodka Badań, Innowacji i Kształcenia (COBIK NIL)
16:15 – Prezentacja projektu „NIL IN”
- Tomasz Rudolf, Ekspert ds. Innowacji NIL, Lider projektu NIL IN
16:30 – Panel dyskusyjny “Od pomysłu do pacjenta – „ścieżka zdrowia” wdrażania innowacji medycznych”
- prof. Grzegorz Basak, twórca Saventic Health i Human Biome Institute
- prof. Piotr Garstecki, twórca Scope Fluidics
- Oskar Kiwic, twórca CardioCube
- Patrycja Wizińska-Socha, Departament Innowacji, Ministerstwo Zdrowia
Moderator: Diana Żochowska, Head of Medonet
17:15 – Panel dyskusyjny „Polska jako hub innowacji medycznych – jak wykorzystać szansę?”
- Aniela Hejnowska, general manager IQVIA
- Tomasz Jaworski, dyrektor Transformacji Cyfrowej Sektora Publicznego, Microsoft
- Robert Ługowski, Cobin Angels
- Karolina Nowak, dyrektor w Agencji Badań Medycznych
- Piotr Najbuk, public & government affairs director, AstraZeneca
Moderator: Jakub Chwiećko, Innovation Lead, EIT Health Innostars, lider grupy roboczej ds. start-upów NIL IN
18:00 – Zakończenie i networking
Relacja z Konferencji na stronie Medycyny Praktycznej ” Lekarz przyszłości – jaki będzie?”
GAZETA LEKARSKA | nr 10 | Październik 2022 – strony 22-25
* “POKIERUJMY pociągiem nowoczesności” Artur Drobniak
d y r e k t o r C e n t r a l n e g o O ś r o d k a B a d a ń ,
I n n o w a c j i i K s z t a ł c e n i a N a c z e l n e j I z b y Lekarskiej
* “CZAS NA INNOWACJE – NIL IN “– powstającej społeczności lekarzy innowatorów – z Tomaszem Rudolfem, ekspertem NIL ds. Innowacji, rozmawia Katarzyna Sadowska-Cioch, zastępca dyrektora Centralnego Ośrodka Badań, Innowacji i Kształcenia Naczelnej Izby Lekarskiej (COBIK NIL).
* Przychodzi pomysł do lekarza, czyli jak budować start-upy medyczne?
SIEĆ I NNOWATORÓW NIL IN – Jakub Chwiećko L i d e r i n n o w a c j i w E I T H e a l t h I n n o S t a r s , s z e f g r u p y r o b o c z e j d s . s t a r t- u p ó w N I L I
Gdzie szukać pomocy:
Centralny Ośrodek Badań, Innowacji i Kształcenia (COBIK NIL) został powołany 2 września 2022 r., na mocy uchwały Nr 20/22/IX Naczelnej Rady Lekarskiej.
Centrum Innowacji i Telemedycyny
NIL-Telemedycyna
ROZWÓJ INNOWACJI MEDYCZNYCH | GDZIE
SZUKAĆ WSPARCIA?
“EIT Health jest europejskim partnerstwem publiczno-prywatnym działającym w obszarze innowacyjnej medycyny i opieki zdrowotnej. W skład naszej siatki wchodzą
wiodące organizacje w dziedzinie edukacji, badań, technologii, ale też szpitale, organizacje pacjenckie i rządowe, pracujące razem nad produktami i rozwiązaniami, które mogą pomóc pacjentom w całej Europie. EIT Health skupia ponad 150 partnerów.
Wśród kluczowych znajdują się m.in.: Roche, AstraZeneca, Amgen, Sanofi Aventis, Abbott, Philips Electronics, GE Healthcare, Danone Nutricia Research, Intel Corporation, jak również Microsoft, Polpharma czy Iqvia w Polsce, a także instytuty badawczo-
-rozwojowe i uniwersytety: Towarzystwo Maxa Plancka, Instytut Karolinska, IESE Business School, Uniwersytety w Sorbonie, Warszawie, Łodzi, Gdańsku oraz Gent.” ( GAZETA LEKARSKA | nr 10 | Październik 2022 str 24-25)
Departament Innowacji Ministerstwa Zdrowia tworzy mapę innowacji.
dr Patrycja Wizińska -Socha w Nestmedic
Pregnabit® Pro umożliwia przeprowadzenie badań teleKTG
Oskar Kiwic – założyciel CardioCube
Obecnie pracuje w USA. O CardioCube
Związki złowonne – odory – diagnostyka zapachu u ludzi.
Zgłaszają się do mnie pacjenci, którzy mają przykry zapach ciała pomimo prawidłowej higieny osobistej. Jest to olbrzymi problem społeczny i osobisty tych osób. Ze względu na zapach ciała tracą przyjaciół, partnerów, pracę co prowadzi do depresji a nawet do myśli samobójczych.
Dla lekarza problemem jest obiektywne stwierdzenie, czy pacjent rzeczywiście wydziela przykry zapach, a jeśli tak, to co go powoduje. Optymalną sytuacją byłoby wykrycie odorowej substancji, a następnie wykrycie, w jaki sposób dostała się lub powstała w organizmie (znalezienie nieprawidłowego szlaku metabolicznego – np. wrodzonego. Mając taką wiedzę można by wyeliminować z diety bądź otoczenia takie związki. Jeśli są one efektem zaburzeń metabolicznych – szukać możliwości naprawy szlaków biochemicznych.
Potrzebujemy więc obiektywnej, standaryzowanej i taniej metody, która pozwoli na wykrycie związku chemicznego w pocie, wydychanym powietrzu lub krwi i moczu pacjenta. Większość substancji zapachowych to substancje organiczne, pozostałe to nieorganiczne.
Rozpocząłem poszukiwania laboratorium, które oznacza takie związki (pisałem o tym na moim blogu). Niestety poza wąskim programem badawczym (trimetylaminuria) PAN z Krakowa (dziękuję za pomoc w i bezpłatnym badaniu mojego pacjenta), badaniem kwasów organicznych w moczu metodą GC/MS substancji obecnych w podstawowych wadach genetycznych i informacjami o halikometrach i sztucznych elektronicznych nosach i GC/MS w ochronie środowiska nie znalazłem placówki wykonującej takie badania. Prosiłem o pomoc Zakład Biochemii Uniwersytetu Medycznego (bez odpowiedzi), Centralnego Laboratorium Komendy Głównej Policji (laboratoria osmologiczne opierają się na węchu psów – ale one jeszcze nie potrafią nazwać związków chemicznych). Podczas rozmowy z chemikami dowiedziałem, że oni też potrafią wyczuć i nazwać śladowe związki chemiczne, ale to nie jest metoda naukowo uznana.
Szukając pomocy wśród znajomych i pacjentów pracujących na Politechnice Łódzkiej dowiedziałem się, że można spróbować wykorzystać do badań spektroskopię absorpcyjną (lub emisyjną) podczerwieni lub ultrafiolecie (jest to dobra i tania metoda) oraz chromatografię gazową ze spektrometrią mas GC/MS
W ten sposób trafiłem do Pani Profesor prof. Beatą Kolesińską z Politechniki Łódzkiej- Instytut Chemii Organicznej, która spróbuje pomóc moim pacjentom badając próbki moczu, potu a może i powietrza. W badaniach będzie można wykorzystać spektrometrię w podczerwieni i GS/MS. Może powstanie program badawczy we współpracy z UM w Łodzi, może firmy kosmetyczne byłyby zainteresowane takimi badaniami? Mój pacjent nawiązał już kontakt z Panią Profesor. Serdecznie dziękują Pani Profesor za zainteresowanie się problemem zapachowym moich pacjentów.
Od Pani Profesor dowiedziałem się, że chemicy nazywają substancje o brzydkim zapach ZŁOWONNYMI. Polecam obszerny artykuł z Narodowego Funduszu Ochrony Środowiska i Gospodarki Wodnej zespołu autorskiego pod kierownictwem prof. dr hab. inż. Jerzy Zwoździak “„Lista substancji i związków chemicznych,które są przyczyną uciążliwości zapachowej”
Warto skorzystać ze stron:
TGSC Information System – (The Good Scents Company) baza zapachów i smaków związków chemicznych
Polecam też wpisy
Szkoła olfaktometrii – Zachodniopomorski Uniwersytet Technologiczny w Szczecinie-Pracownia Zapachowej Jakości Powietrza działa na Wydziale Technologii i Inżynierii Chemicznej PS
Odory – Joanna Kośmider, Barbara Mazur-Chrzanowska, Bartosz Wyszyński -PWN 2021
Melioidoza, Orientia tsutsugamushi i inne „pamiątki z wakacji” – zbadasz w Hamburgu – BNITM
Jesteśmy przed sezonem wakacyjnym. Z wyjazdów zagranicznych oprócz wrażeń i opalenizny czasem przywozimy choroby, które są pamiątką na całe życie. Niektórych z nich nie ma możliwości rozpoznania w naszych laboratoriach. Mamy hipotezę, ale potwierdzenia brak. Szukamy w laboratoriach weterynaryjnych, wojskowych z bronią biologiczną – nikt nie oznacza.
Diagnostyka trudnych przypadków daje mi możliwość współpracy z pacjentami, którzy dzięki swojej wytrwałości znajdują na świecie odpowiednie laboratoria (są to dni przeszukiwania Internetu, kontaktów ze specjalistami z krajów, w których doszło do zakażenia -np. Tajlandia), opłacania zdalnych konsultacji laboratoryjnych jak np. Szpital Medycyny Tropikalnej w Holandii – i … NIC !!.
Wśród chorób tropikalnych, o trudnej diagnostyce znajduje się już wcześniej opisywana przeze mnie na blogu Melioidoza (burkholderia pseudomallei), którą można „przywieźć” z Tajlandii.
Dlatego chcę pokazać zestaw badań w laboratorium, które wykonuje dość szeroki zestaw w zakresie chorób tropikalnych. Jest nim:
Bernhard-Nocht-Institut für Tropenmedicin
Zentrale Labordiagnostic Fachärtze für Mikrobiologie, Virologie und Infektionsepidemiologie, Prof. Dr. Stephan Günther, Prof. Dr. Dennis Tappe
Bernhard-Nocht-Str. 74 – 20359 Hamburg
Tel. +49 40 42818-211 (Ärtze), -252 Fax
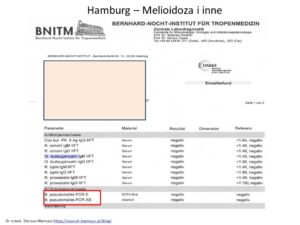
 Dzięki uprzejmości i za zgodą pacjentki przedstawiam zestaw badań wykonywanych w BNITM w 2022 r.
Dzięki uprzejmości i za zgodą pacjentki przedstawiam zestaw badań wykonywanych w BNITM w 2022 r.
Wśród mało u nas znanych chorób ( zobacz mapkę rozprzestrzenienia choroby – Tsutsugamushi_Triangle) (obszar występowania wewnątrz trójkąta Iran-Japonia-Australia) chorób diagnozowanych przez to laboratorium w Hamburgu znajduje się też m.in.
Orientia tsutsugamushi (Wikipedia)
One billion people are estimated to be at risk of infection at any moment and an average of one million cases occur every year in the Tsutsugamushi Triangle.
“Orientia tsutsugamushi (from Japanese tsutsuga meaning “illness”, and mushi meaning “insect”) is a miteborne bacterium belonging to the family Rickettsiaceae and is responsible for a disease called scrub typhus in humans.[1] It is a natural and an obligate intracellular parasite of mites belonging to the family Trombiculidae Orientia tsutsugamushi causes a complex and potentially life-threatening disease known as scrub typhus. Infection starts when chiggers bite on the skin during their feeding. The bacteria are deposited at the site of feeding (inoculation), where they multiply. They cause progressive tissue damage (necrosis), which leads to formation of an eschar on the skin. Necrosis progresses to inflammation of the blood vessels, called vasculitis. This in turn causes inflammation of the lymph nodes, called lymphadenopathy. Within a few days, vasculitis extends to various organs including the liver, brain, kidney, meninges and lungs.[56] The disease is responsible for nearly a quarter of all the febrile (high fever) illness in endemic areas. Mortality in severe cases or due to improper treatment or misdiagnosis may be as high as 30-70%.[57] About 6% of infected people die untreated, and 1.4% of the patients die even with medical treatment. Moreover, the death rate can be as high as 14% with neurological problems and 24% with multi-organ dysfunction among treated patients.[58] In cases of misdiagnosis and failure of treatment, systemic complications rapidly develop including acute respiratory distress syndrome, acute kidney failure, encephalitis, gastrointestinal bleeding, hepatitis, meningitis, myocarditis, pancreatitis, pneumonia, septic shock, subacute thyroiditis, and multiple organ dysfunction syndrome.[59]
Harmful effects involving multiple organ failure and neurological impairment are difficult to treat, and can cause lifelong debilitation or be directly fatal.[59] The central nervous system is often affected and results in various complications including cerebellitis, cranial nerve palsies, meningoencephalitis, plexopathy, transverse myelitis, and Guillan-Barre syndrome.[60] Death rates due to complications can be up to 14% in brain infections, and 24% with multiple organ failure.[58] In India, scrub typhus has become the major cause of acute encephalitis syndrome, which was earlier caused mainly by a viral infection, Japanese encephalitis.[61]”.
Uporczywy świąd – Rtg klatki piersiowej – chłoniak Hodgkina.
Chłoniak Hodgkina (dawniej ziarnica złośliwa)
Z pewnością wielu z nas zdarzyło się szukać jakiegoś przedmiotu wśród wielu innych rzeczy i nie widzieć go, mimo, że znajdował się tuż przed naszymi oczami (Słynny “Pan Hilary“). Dopiero jak ktoś pokazał nam przedmiot, dziwiliśmy się, że mogliśmy go nie zauważyć (Jak okulary “na własnym nosie” 🙂 )
Podobnie bywa też w medycynie, jak ktoś powie nam (jak opisałem w tytule tego artykułu), że u pacjenta ze świądem skóry (bez zmian skórnych i powiększonych obwodowych węzłów chłonnych) czasem może być chłoniak Hodgkina zlokalizowany w klatce piersiowej, a wykonanie rtg klatki piersiowej za 50 zł umożliwi postawienie ostatecznego rozpoznania, to cóż prostszego – zlecamy rtg i problem rozwiązany.
Badanie rtg klatki piersiowej kiedyś obowiązkowo i rutynowo wykonywane co roku mogłoby wykryć taką chorobę.
Dlatego też analizując “trudne przypadki diagnostyczne” rozpoczynam pracę od żmudnej analizy i uporządkowania dotychczasowej dokumentacji. Sprawdzam, jakie badania wykonano wcześniej, czy były jakieś odchylenia od normy, które badania pominięto (szczególnie badania podstawowe – rtg klatki, usg brzucha, badania moczu i morfologii krwi).
Niestety na taka analizę nie wystarczy 15-30 minut w gabinecie. Sporządzenie mojej dokumentacji zajmuje mi nawet 10 godzin (w zależności od ilości dokumentów i wykonanych badań).
Właśnie taka analiza pozwoliła mi w ustaleniu rozpoznania chłoniaka Hodgkina u 40 letniej pacjentki. Chora od lat była leczona przez dermatologów z powodu łuszczycy, miała wiele problemów osobistych (stąd sugerowano psychiczne podłoże choroby), od 2019 roku (czyli od 3 lat) zgłaszała uporczywy świąd skóry, w miejscach, w których nie było zmian skórnych. Sprawę komplikował fakt, że choroba rozpoczęła się tuż po przeprowadzeniu do starego (ale wyremontowanego) mieszkania. Ponadto pacjentka dużo podróżowała po świecie. Dolegliwości nasilały się przy kontakcie z blatami mebli i farbowaną skórą. Były także inne objawy jak nadmierne pocenie się, rogowacenie skóry dłoni i stóp, bezsenność, rozdrażnienie, brak koncentracji, nadmierne zmęczenie, depresja.
Problemem dodatkowym było to, że pacjentka miała długoletni wywiad dermatologiczny (łuszczyca), była leczona przez wielu lekarzy oraz w klinice dermatologicznej. Stosowano leki antyhistaminowe, ale także przeciw świerzbowi. Z powodu świądu chora nie była w stanie nawet nosić ubrań (w domu chodziła tylko w bieliźnie), poza domem nosiła luźne rzeczy, czy wyjątkowo różniła się od otoczenia. Stosowane leczenie nie przynosiło poprawy.
Z mojej analizy wynikało, że należy między innymi brać pod uwagę choroby układu chłonnego, choroby alergiczne, zespoły paranowotworowe, zaburzenia metaboliczne, choroby pasożytnicze.. W dotychczasowej dokumentacji nie znalazłem wyniku badania radiologicznego klatki piersiowej. Dlatego m.in. zleciłem takie RTG .
Po badaniu diagnostyka poszła już błyskawicznie. Rozpoznano powiększenie węzłów chłonnych śródpiersia. Chora konsultowana przez hematologów – wykonano biopsję węzłów chłonnych- rozpoznano chłoniak Hodgkina. Chora właśnie rozpoczyna terapię celowaną.
COVID-19, D-dimery i …. zakrzep w tętniaku tętnicy podkolanowej.
Czasem z algorytmów wynika jedno, a znajdujemy niespodziewane rozpoznanie.
Ostatnio diagnozowałem pacjenta w wieku 70 lat, wcześniej przez wiele lat pracował w pozycji stojącej. Chory skarżył się na złe samopoczucie po przebytej przed miesiącem infekcji Sars Cov-2. Bez duszności, bez krwioplucia. Pacjent ma z żylaki podudzi.
Zleciłem między innymi oznaczenie D-dimerów. Wynik – 3370 (norma<500). Spodziewając się zakrzepowych zmian w żylakach kończyn dolnych i być może towarzyszącej jej zatorowości płucnej zleciłem badanie USG Dopppler naczyń kończyn dolnych.
Ku mojemu zaskoczeniu – w żyłach nie stwierdzono zmian zakrzepowych, ale … stwierdzono na lewej tętnicy podkolanowej tętnik wielkości ok. 7 mm ze zmianą zakrzepową.
Medycyna często wymyka się spod statystyk i uczy pokory. Nie zawsze to co najczęstsze i w algorytmie lub wytycznych powoduje chorobę. Trzeba szukać i myśleć szerzej.
Tak więc: “Szukajcie, a znajdziecie”. Tylko, że możemy znaleźć to, czego nie szukaliśmy :).